AMH-RII: visión molecular de problemas hormonales en la diferenciación sexual
En el ser humano, la sexta semana del desarrollo embrionario marca el inicio de la diferenciación de los conductos genitales. En el embrión masculino, se genera una hormona que produce la degeneració de los conductos de Müller (la hormona anti-mülleriana AMH), sin la acción represora de la cual, estos conductos llevarían a la generación de las trompes y la matriz. Una parte importante de la represión de esta hormona se basa en procesos de fijación en las membranas celulares, gracias a un receptor específico (el AMH-RII). Cualquier error en estos procesos que involucran tanto a la hormona como a su receptor, puede dar lugar a un singular fenómeno de hermafroditismo. Un equipo de investigadores de la UAB ha podido elaborar una modelización tridimensional del receptor de la hormona que facilitará el estudio de las diferentes mutaciones que puede sufrir y, por lo tanto, la comprensión de esta extraña enfermedad genética.
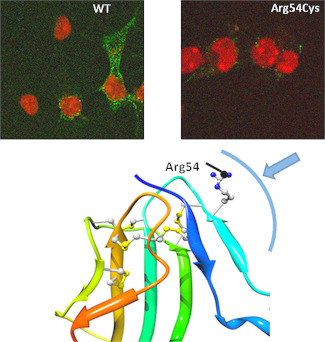
La hormona anti-mülleriana (AMH) tiene un papel fundamental en el proceso de desarrollo sexual del embrión masculino por su acción represora sobre los conductos de Müller, unos conductos presentes en los embriones de ambos sexos y que, al desarrollarse, generan parte de los órganos genitales femeninos (trompas y matriz). Esta represión involucra un mecanismo molecular complejo, que va desde la fijación de la AMH a la superficie de las células de los conductos de Müller hasta la fijación de unos complejos proteicos sobre unos genes específicos del DNA nuclear. Situado encima la membrana celular, el receptor de la hormona anti-mülleriana de tipo II (AMH-RII) es clave en este mecanismo puesto que está involucrado en la fijación de la hormona (en la parte extracelular del receptor) y en la activación de los primeros enzimas intracelulares que traerán el mensaje hacia el núcleo (parte intracelular de AMH-RII). Cualquier error en la cascada de acontecimientos moleculares asociados al AMH lleva a un singular fenómeno de hermafrodisme, conocido como Síndrome de Conducto de Müller Persistente (SCMP) y caracterizado por la existencia de conductos de Müller más o menos desarrollados en individuos correctamente masculinizados.
El equipo de la Prof. di Clemente del Institut National de la Santé et de la Recherche Médicale (Francia) estudia la SCMP desde hace más 25 años y, actualmente, es el único equipo en el mundo que censa los casos de manera sistemática, analiza el genoma de los pacientes afectados y, a la vez, intenta entender los mecanismos moleculares implicados. Su trabajo ha mostrado que, de 114 mutaciones caracterizadas, más del 80% afectan al gen de la hormona misma o al del receptor. Hasta ahora, no obstante, la ausencia de estructuras tridimensionales de estas especies limitaba la racionalización a nivel molecular del efecto de estas mutaciones.
Investigadores del Dep. de Química y de el Instituto de Biomedicina y Biotecnología de la UAB, pudieron dar una primera visión atómica de una serie de mutaciones de la AMH-RII relacionadas con la SCMP. Mediante el uso de técnicas de modelización por homologia y de dinámica molecular, generaron unos modelos tridimensionales del AMH-RII. Esta modelización se ha basado en estructuras de especies homólogas disponibles en la base de datos cristalográficos de proteínas. Comparando datos experimentales y los modelos, se muestra que las mutaciones estudiadas del receptor tienen consecuencias moleculares muy diversas. Ciertas mutaciones (en la parte extracelular) disminuyen radicalmente la capacidad de fijación de la hormona en el receptor debido a un cambio conformacional en la región de reconocimiento. Otros (parte intracelular), desestabilizan la estructura de la proteína, distorsionan la zona de fosforilación o modifican las propiedades de reconocimiento de otros receptores implicados en la cadena de transmisión del señal.
Este trabajo multidisciplinario permite un mejor conocimiento de las bases moleculares de una enfermedad genética rara. Los modelos estructurales generados constituyen una base de trabajo para el estudio de nuevas mutaciones, así como para el diseño de experimentos para el estudio más en detalle de la transmisión de la señal de la AMH.
Referencias
"Natural mutations of the anti-Mullerian hormone type II receptor found in persistent Mullerian duct syndrome affect ligand binding, signal transduction and cellular transport". Belville, C; Maréchal, J-D; Pennetier, S; Carmillo, P; Masgrau, L; Messika-Zeitoun, L; Galey, J; Machado, G; Treton, D; Gonzales, J; Picard, JY; Josso, N; Cate, RL; di Clemente, N. HUMAN MOLECULAR GENETICS, 18 (16): 3002-3013 AUG 15 2009.